Regeringsuppdrag om MDR och IVDR – stärkt stöd till branschen och tydligare svensk röst i EU
2.3.2026 07:45:00 CET | Läkemedelsverket | Pressmeddelande
Läkemedelsverket har nu redovisat sitt regeringsuppdrag om att underlätta implementeringen av EU:s regelverk för medicintekniska produkter (MDR) och medicintekniska produkter för in vitro-diagnostik (IVDR). Arbetet har omfattat 13 olika aktiviteter med bland annat informationsinsatser, stärkt dialog med branschen och åtgärder för att öka tillgängligheten till anmälda organ i Sverige.
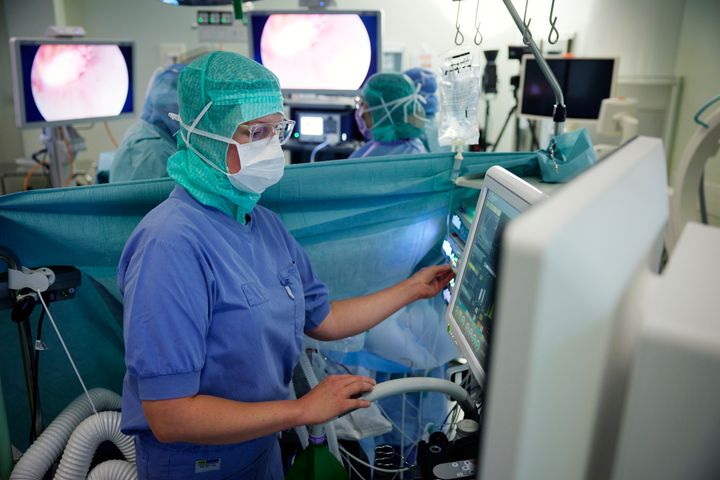
Uppdraget, som gavs i december 2024, har tre delar:
- att ge information och rådgivning till aktörer
- att verka för att svenska ståndpunkter tas tillvara i EU-arbetet samt
- att möjliggöra för fler anmälda organ inom landet.
– I arbetet med detta uppdrag har Läkemedelsverket strävat efter ett helhetsperspektiv över utmaningarna, och arbetet har omfattat insatser på såväl nationell som europeisk nivå. I uppdraget har vi till exempel arbetat för att förenkla och förtydliga regelverkens tillämpning, och utveckla former för återkoppling från tillsyn, säger Lena Björk, direktör för verksamhetsområde medicinteknik på Läkemedelsverket.
Fördjupat informationsstöd
Läkemedelsverket har genomfört en oberoende kommunikationsanalys som lägger grunden för mer träffsäker och effektiv kommunikation inom medicinteknikområdet. Under uppdraget har även nya verktyg och arbetssätt testats och optimerats för webbinarier och videobaserade e-kurser på Läkemedelsverkets utbildningsportal.
Andra insatser är översättning av webbinformation till engelska, stöd kopplat till branschens användning av Eudamed, som är den europeiska databasen för medicintekniska produkter, och rutiner för att publicera samlade tillsynserfarenheter. Myndigheten har också prövat nya former för regulatorisk rådgivning inom ramen för ett medicintekniskt innovationsstöd.
Aktivt EU-arbete och strukturerad branschdialog
Inom den europeiska delen av uppdraget har myndigheten fokuserat på områden med särskilt stor påverkan på implementeringen, däribland den riktade utvärderingen av MDR och IVDR, krav på anmälda organ och samordnade bedömningar av kliniska prövningar respektive prestandastudier. Läkemedelsverket är fortsatt mycket aktiva i förhandlingarna gällande översynen av regelverken på EU-nivå.
Strukturerade branschdialoger har startats upp för att samla in svenska erfarenheter och ståndpunkter. Dessa används både i det nationella arbetet och i EU-samarbetet.
Åtgärder för att stärka tillgången till anmälda organ
Myndigheten har också vidtagit åtgärder som syftar till att öka tillgängligheten till svenska anmälda organ. Bland annat har arbete inletts för att kunna bedöma anmälda organ gällande certifieringsaktiviteter inom reprocessing av medicintekniska engångsprodukter – ett område där EU-vägledning i dagsläget saknas.
Förslag om permanent stöd och fortsatta satsningar
I rapporten föreslås fyra åtgärder för att säkerställa långsiktig effekt:
- Varaktiga resurser för fortsatt implementeringsstöd.
- Inrättande av ett permanent medicintekniskt innovationsstöd.
- Etablering av strukturerade branschdialoger inom medicinteknik.
- Se över Läkemedelsverkets mandat att utse anmälda organ avseende reprocessing.
– Vår samlade bedömning är att arbetet har skapat bättre förutsättningar för en enhetlig och effektiv tillämpning av MDR och IVDR i Sverige. Samtidigt konstateras att förväntningarna på fortsatt stöd är stora och att arbetet därför bör ges en direkt fortsättning, avslutar Lena Björk.
Nyckelord
Kontakter
Läkemedelsverkets presstjänst
Tel:018-18 36 25press@lakemedelsverket.seBilder
Länkar
Läkemedelsverket arbetar för att patienten, hälso- och sjukvården samt djursjukvården får tillgång till säkra och effektiva produkter och att de används ändamålsenligt och effektivt. Läkemedelsverkets vision är att vara en ledande kraft i samverkan för bättre hälsa.
Följ Läkemedelsverket
Abonnera på våra pressmeddelanden. Endast mejladress behövs och den används bara här. Du kan avanmäla dig när som helst.
Senaste pressmeddelandena från Läkemedelsverket
Myndigheternas beslut vilar på vetenskap och EU-gemensamma bedömningar28.2.2026 10:01:31 CET | Pressmeddelande
Läkemedelsverket uppmanar i en replik i Svenska Dagbladet Jacob Lindberg och Per Sjöberg, båda med intressen i Oncopeptides, att skyndsamt publicera eventuella bevis för sina påståenden om forskningsfusk kopplat till cancerläkemedlen imider.
Var tredje person har sett falska läkemedelsannonser i sociala medier – viktnedgångsprodukter vanligast vid bluffköp24.2.2026 10:17:58 CET | Pressmeddelande
Vilseledande annonser om läkemedel i sociala medier är ett problem, det ger en ny Novusundersökning stöd för. Drygt en av tre (35 procent) uppger att de under de senaste 12 månaderna har sett en annons om ett läkemedel i sociala medier som de misstänkt varit en bluff.
Läkemedelsverkets årsredovisning för 202523.2.2026 10:55:00 CET | Pressmeddelande
Oron i omvärlden med ökade krav på beredskap och säkerhet präglade också Läkemedelsverkets 2025. Myndigheten fortsatte arbetet med att både stärka den egna beredskapsorganisationen och bidraget till ett motståndskraftigt samhälle.
Det nordiska språkprojektet fyller ett år och fortsätter att expandera19.2.2026 13:03:00 CET | Pressmeddelande
Pilotprojektet för engelskspråkiga gemensamma nordiska förpackningar för utvalda sjukhusläkemedel är i gång sedan drygt ett år, med ett ökande antal produkter som inkluderas
Förslag ska göra det lättare för patienter att få läkemedel vid bristsituationer17.2.2026 06:11:00 CET | Pressmeddelande
I sin slutrapport om åtgärder för att förebygga och hantera rest- och bristsituationer presenterar Läkemedelsverket flera förslag som stärker apotekens möjligheter att agera när läkemedel inte räcker till. Förslagen syftar till att fler patienter ska få tillgång till behandling även vid läkemedelsbrist – utan att patientsäkerheten äventyras.
I vårt pressrum kan du läsa de senaste pressmeddelandena, få tillgång till pressmaterial och hitta kontaktinformation.
Besök vårt pressrum