Regeringsuppdrag om MDR och IVDR – stärkt stöd till branschen och tydligare svensk röst i EU
2.3.2026 07:45:00 CET | Läkemedelsverket | Pressmeddelande
Läkemedelsverket har nu redovisat sitt regeringsuppdrag om att underlätta implementeringen av EU:s regelverk för medicintekniska produkter (MDR) och medicintekniska produkter för in vitro-diagnostik (IVDR). Arbetet har omfattat 13 olika aktiviteter med bland annat informationsinsatser, stärkt dialog med branschen och åtgärder för att öka tillgängligheten till anmälda organ i Sverige.
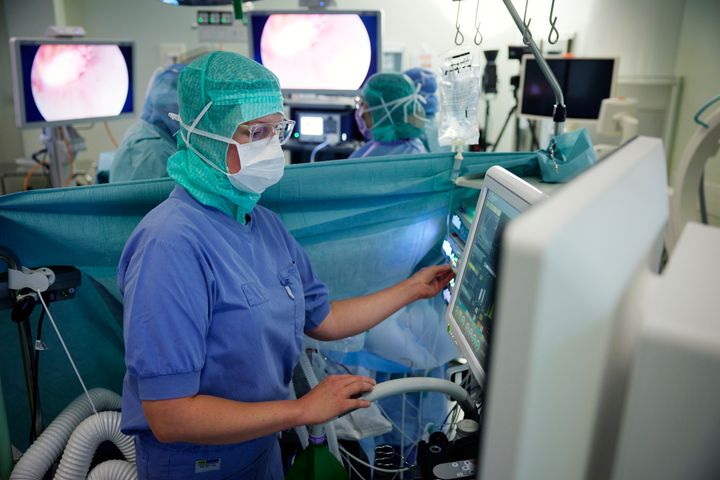
Uppdraget, som gavs i december 2024, har tre delar:
- att ge information och rådgivning till aktörer
- att verka för att svenska ståndpunkter tas tillvara i EU-arbetet samt
- att möjliggöra för fler anmälda organ inom landet.
– I arbetet med detta uppdrag har Läkemedelsverket strävat efter ett helhetsperspektiv över utmaningarna, och arbetet har omfattat insatser på såväl nationell som europeisk nivå. I uppdraget har vi till exempel arbetat för att förenkla och förtydliga regelverkens tillämpning, och utveckla former för återkoppling från tillsyn, säger Lena Björk, direktör för verksamhetsområde medicinteknik på Läkemedelsverket.
Fördjupat informationsstöd
Läkemedelsverket har genomfört en oberoende kommunikationsanalys som lägger grunden för mer träffsäker och effektiv kommunikation inom medicinteknikområdet. Under uppdraget har även nya verktyg och arbetssätt testats och optimerats för webbinarier och videobaserade e-kurser på Läkemedelsverkets utbildningsportal.
Andra insatser är översättning av webbinformation till engelska, stöd kopplat till branschens användning av Eudamed, som är den europeiska databasen för medicintekniska produkter, och rutiner för att publicera samlade tillsynserfarenheter. Myndigheten har också prövat nya former för regulatorisk rådgivning inom ramen för ett medicintekniskt innovationsstöd.
Aktivt EU-arbete och strukturerad branschdialog
Inom den europeiska delen av uppdraget har myndigheten fokuserat på områden med särskilt stor påverkan på implementeringen, däribland den riktade utvärderingen av MDR och IVDR, krav på anmälda organ och samordnade bedömningar av kliniska prövningar respektive prestandastudier. Läkemedelsverket är fortsatt mycket aktiva i förhandlingarna gällande översynen av regelverken på EU-nivå.
Strukturerade branschdialoger har startats upp för att samla in svenska erfarenheter och ståndpunkter. Dessa används både i det nationella arbetet och i EU-samarbetet.
Åtgärder för att stärka tillgången till anmälda organ
Myndigheten har också vidtagit åtgärder som syftar till att öka tillgängligheten till svenska anmälda organ. Bland annat har arbete inletts för att kunna bedöma anmälda organ gällande certifieringsaktiviteter inom reprocessing av medicintekniska engångsprodukter – ett område där EU-vägledning i dagsläget saknas.
Förslag om permanent stöd och fortsatta satsningar
I rapporten föreslås fyra åtgärder för att säkerställa långsiktig effekt:
- Varaktiga resurser för fortsatt implementeringsstöd.
- Inrättande av ett permanent medicintekniskt innovationsstöd.
- Etablering av strukturerade branschdialoger inom medicinteknik.
- Se över Läkemedelsverkets mandat att utse anmälda organ avseende reprocessing.
– Vår samlade bedömning är att arbetet har skapat bättre förutsättningar för en enhetlig och effektiv tillämpning av MDR och IVDR i Sverige. Samtidigt konstateras att förväntningarna på fortsatt stöd är stora och att arbetet därför bör ges en direkt fortsättning, avslutar Lena Björk.
Nyckelord
Kontakter
Läkemedelsverkets presstjänst
Tel:018-18 36 25press@lakemedelsverket.seBilder
Länkar
Läkemedelsverket arbetar för att patienten, hälso- och sjukvården samt djursjukvården får tillgång till säkra och effektiva produkter och att de används ändamålsenligt och effektivt. Läkemedelsverkets vision är att vara en ledande kraft i samverkan för bättre hälsa.
Följ Läkemedelsverket
Abonnera på våra pressmeddelanden. Endast mejladress behövs och den används bara här. Du kan avanmäla dig när som helst.
Senaste pressmeddelandena från Läkemedelsverket
Huggormen är vaken – agera snabbt om du blir biten7.5.2026 07:30:00 CEST | Pressmeddelande
Att huggormarna nu vaknat av värmen är tydligt. Nu ökar samtalen om huggormsbett till Giftinformationscentralen. Uppemot 400 personer vårdas varje år på sjukhus till följd av huggormsbett. Många behöver motgift.
Nytt regeringsuppdrag utreder barnmorskors möjlighet att förskriva abortläkemedel4.5.2026 13:46:09 CEST | Pressmeddelande
Regeringen ger Socialstyrelsen och Läkemedelsverket i uppdrag att utreda om, och i så fall hur, barnmorskor ska få förskriva läkemedel som används vid abort.
Sex procent ändrar sin medicinering efter råd i sociala medier4.5.2026 07:30:00 CEST | Pressmeddelande
En undersökning från Novus, genomförd på uppdrag av Läkemedelsverket, visar att sex procent av svenskarna har ändrat sin läkemedelsanvändning baserat på information från sociala medier under det senaste året. Bland män i åldern 65–84 år är siffran ännu högre. Nu betonar Läkemedelsverket vikten av att inte ändra sin läkemedelsbehandling utan att rådgöra med apoteks- eller vårdpersonal vid frågor och att läsa läkemedlets bipacksedel.
Sommarvärmen drar in: Hög tid att se över ditt solskydd29.4.2026 07:00:00 CEST | Pressmeddelande
När en ny värmebölja rullar in över landet påminner Läkemedelsverket om vikten av rätt solskydd. En undersökning från Novus visar att endast var tredje svensk i första hand använder skugga och kläder som skydd – trots att det är de mest effektiva metoderna för att undvika hudskador.
EU:s bioteknikförslag behöver stärkas för att säkra patientsäkerhet28.4.2026 07:03:00 CEST | Pressmeddelande
Läkemedelsverket ställer sig positivt till EU-kommissionens ambition att stärka bioteknik och klinisk forskning, men varnar samtidigt för att delar av förslaget riskerar att försämra kvaliteten i prövningar och i förlängningen påverka patientsäkerheten.
I vårt pressrum kan du läsa de senaste pressmeddelandena, få tillgång till pressmaterial och hitta kontaktinformation.
Besök vårt pressrum